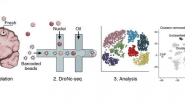
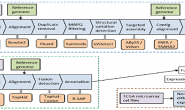
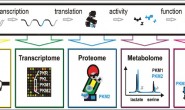
السلام عليكم ورحمة الله تعالى وبركاته, تكلمنا في مقالات سابقة عن بعض مفاهيم علم الوراثة اللاجينية (epigenetics), كالتعديلات الاجينية التي تتم عن طريق ارتباط البروتينات بالجينوم أو التغيرات الكيميائية التي تَحدث على أذناب الهستونات أو حتى عن طريق التغيُرات في البنية التَشكيلية للجينوم. في هذا المقال سوف نتطرق إلى نوع آخر من بيانات علم الوراثة الاجينية والذي يتعلق بدراسة المناطق المفتوحة من الكروماتين (يصطلح عليها أيضا : إتاحة الكروماتين أو Chromatin accessibility). هذا النوع من البيانات يعتبر تكميليا لبيانات الوراثة الاجينية التي يمكننا التحصل عليها باستعمال تقنيات السلسلة (كتقنية الـ ChP-seq و Hi-C) و يساعدنا في تكوين نظرة شبه شاملة عن التعديل الاجيني بتكلفة اقل ودقة عالية.
سوف نحاول إذا في هذا المقال شرح أهمية إتاحة الكروماتين وعلاقتها بتعديل التعبير الجيني ثم سوف نتطرق إلى بعض طرق تنميط اتاحة الكروماتين الشائعة في أوساط البحث العلمي.
علاقة إتاحة الكروماتين بالتعديل الجيني
على الرغم من التمايز الوظيفي بين خلايا الكائن الواحد, إلا أنها تحتوي كلها على نفس الحمض النووي. لهذا فان التمايز الوظيفي بين خلايا الكائن الواحد لا يتم عن طريق التمايز في الحمض النووي لكن يتم عن طريق التمايز في التغيُرات اللاجينية لجينوماتها. تتحكم هذه التغيرات الاجينية بدقة عالية في التعبير الجيني للخلية عن طريق تنشيط أو تثبيط بعض الجينات وبالتالي تساهم في تحديد سلوك الخلية.
كما أسلفنا في المقالات السابقة, يتم التعديل الاجيني لنشاط الجينات عن طريق التحكم في كمية إنضغاط و إنفتاح الكروماتين (حمض نووي + هستونات) خاصة في المناطق المُنظِمة (Regulatory regions) كالمُحفِزَات (Promoters) و المُغزِزَات (Enhancers).
ُيسهل انفتاح الكروماتين وُلوجَ عوامل النسخ (Transcription factors) التي تستقطب انزيم الارنا بوليميراز2 (RNA Pol-II) إلى المحفزات مما يؤدي إلى تفعيل عملية النسخ للجين. في المقابل, المناطق المضغوطة من الجينوم تعيق ولوج عوامل النسخ وبالتالي تثبيط التعبير الجيني. على الرغم من ان المناطق المفتوحة تمثل 3% من الجينوم, الا انها تحتوي على حوالي 90% من مناطق إرتباط عناصر النسخ (Transcription factors binding sites).
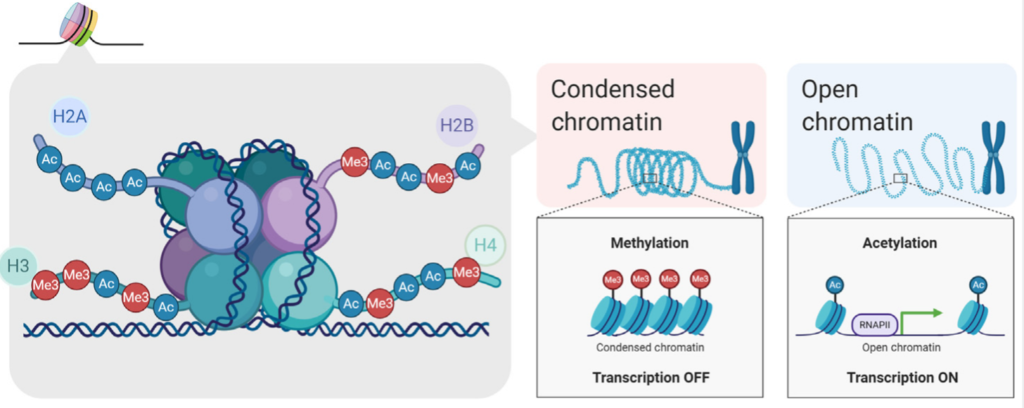
رسم بياني يوضح علاقة اتاحة الكروماتين بالتعديل الجيني (مصدر الصورة)
يساهم انفتاح الكروماتين ايضا في تغير البنية الثلاثية للجينوم, حيث انه يسمح بارتباط البروتينات التشكيلية (Architectural proteins) كـ CTCF بالمناطق المفتوحة في الجينوم مما يؤدي الى تشكل عروات الكروماتين (Chromatin loops) وتسهيل التواصل بين المحفزات ومعززاتها التي قد تتواجد في مناطق جينومية بعيدة.
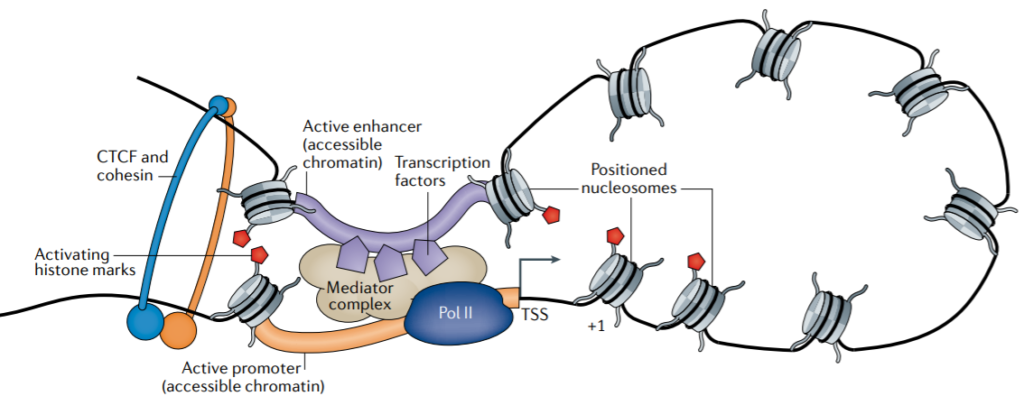
رسم بياني يوضح علاقة اتاحة الكروماتين بالبنية الثلاثية للجينوم (مصدر الصورة)
العوامل المؤثرة على ازاحة الكروماتين
هناك عدة عوامل تؤثر على ازاحة الكروماتين, من بيته :
- تعديل الهستونات (Histone modification): يمكن لبعض التعديلات على الهستونات كالأستلة (Acetylation) والمثيلة (methylation) أن تجعل الوصول إلى الحمض النووي أكثر سهولة وتعزز التعبير الجيني. على سبيل المثال ، يمكن أن تؤدي أستلة اذناب اللايسين على الهستونات إلى إضعاف الارتباط بين الهيستونات والحمض النووي وتسهيل ولوج عوامل النسخ والعوامل الاخرى الى الحمض النووي وبالتالي التاثير على ازاحة الكروماتين. اظافة الى ذلك, تعد تعديلات هيستون ديناميكية ويمكن عكسها ، مما يسمح بضبط التعبير الجيني استجابةً للإشارات الخلوية المختلفة.
- إعادة تشكيل الكروماتين (Chromatin remodeling): يمكن أن تغير إنزيمات إعادة تشكيل الكروماتين (Chromatin remodeling enzymes) بنية الكروماتين عن طريق تحريك الهستونات أو إضافتها أو إزالتها أو عن طريق تعديل الهيستونات نفسها وبالتالي التاثير على ازاحة الكوماتين.
- مثيلة الحمض النووي (DNA methylation): بشكل عام ، تميل مناطق الجينوم التي تحتوي على مستويات عالية من مثيلة الحمض النووي إلى امتلاك مستويات أقل من الكروماتين المفتوح والتعبير الجيني المنخفض ، بينما تميل المناطق ذات المستويات المنخفضة من مثيلة الحمض النووي إلى امتلاك مستويات أعلى من الكروماتين المفتوح والتعبير الجيني العالي. ومع ذلك ، فإن هذه العلاقة ليست دائمًا مباشرة ، ويمكن أن تختلف العلاقة بين الكروماتين المفتوح ومثيلة الحمض النووي والتعبير الجيني اعتمادًا على السياق المحدد ونوع الخلية. وجدت بعض الدراسات أن مثيلة الحمض النووي يمكن أن تؤثر على إمكانية وصول الحمض النووي إلى آلية النسخ ، ربما عن طريق التأثير على ارتباط عوامل النسخ أو البروتينات التنظيمية الأخرى بالحمض النووي. اقترحت دراسات أخرى أن الكروماتين المفتوح ومثيلة الحمض النووي يمكن تنظيمها من خلال آليات مشتركة ، مثل نشاط الإنزيمات التي تعدل الهيستونات أو الحمض النووي.
- الحمض النووي الريبي غير المشفر (ncRNAs): الحمض النووي الريبي غير المشفر عبارة عن جزيئات من الحمض النووي الريبي التي لا تنتج بروتينات. يمكن لبعض ncRNAs الارتباط بمناطق معينة من الحمض النووي والتأثير على إمكانية وصول الحمض النووي إلى عوامل النسخ والبروتينات التنظيمية الأخرى. هناك علاقة معقدة بين ازاحة الكروماتين و RNAs غير المشفر. يمكن لبعض RNAs غير المشفرة ، مثل RNAs الطويلة غير المشفرة (lncRNAs) ، الارتباط بمناطق معينة من الجينوم والتأثير على بنية الكروماتين ، مما يجعل الوصول إلى الحمض النووي أكثر أو أقل لعوامل النسخ والبروتينات التنظيمية الأخرى. على سبيل المثال ، يمكن لـ lncRNAs ان تستقطب إنزيمات إعادة تشكيل الكروماتين أو البروتينات التنظيمية الأخرى إلى مناطق جينومية معينة ، مما يؤثر على إمكانية وصول الحمض النووي إلى آلية النسخ.
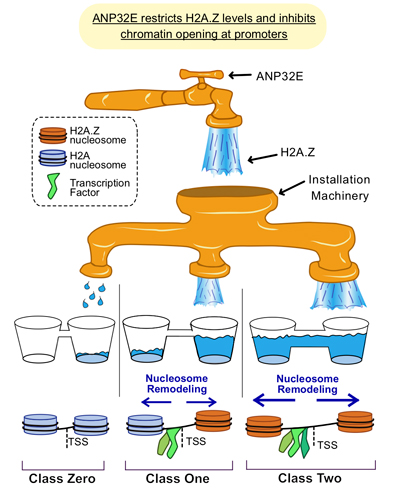
رسم توضيحي يبين علاقة انزيمات اعادة تشكيل الكروماتين بازاحة الكروماتين (مصدر الصورة)
طرق دراسة مناطق ازاحة الكروماتين
سمحت تقنيات الجيل الجديد للسلسلة (NGS technologies) للباحثين من تطوير آليات عديدة لدراسة مناطق ازاحة الكروماتين على نطاق الجينوم باكمله. من بين اهم هذه التقنيات هي:
- FAIRE-seq (عزل العناصر التنظيمية بمساعدة الفورمالديهايد): تعد من اقدم هذه التقنيات و الاقل استعمالا. تعتمد طريقة FAIRE-seq على استعمال الفورمالدهيد لتثبيت المناطق المرتبطة بالبرونات, ثم استخدام طريقة الصوتنة لتقطيع الحمض النووي ثم استخلاص المناطق الحرة عن طريق استعمال طريقة الفصل بين الفينول والكلوروفورم. على الرغم من سهولة هذه الطريقة الا انها لا تعطينا بيانات ذات نوعية جيدة وتقريبا لا يتم استعمالها حاليا.
- DNase-seq (سلسلة مناطق DNase I): تتضمن هذه الطريقة معالجة الخلايا بإنزيم DNase I ، الذي يقطع الحمض النووي بشكل انتقائي في مواقع الكروماتين المفتوحة. يتم بعد ذلك تسلسل أجزاء الحمض النووي الناتجة لرسم خريطة لمناطق الكروماتين المفتوحة. تعتبر هذه التنقية من التقنيات الرائجة في مجال دراسة ازاحة الكروماتين واستعملت بكثرة في مشروع ENCODE.
- ATAC-seq (سلسلة المناطق المتاحة للترانسبوزاز): تتضمن هذه الطريقة استخدام إنزيم Tn5 transposase لإدخال محولات التسلسل (adapter sequences) في مناطق الكروماتين المفتوحة. يتعرف Tn5 على مناطق الكروماتين المفتوحة بناءً على إمكانية وصولها إلى الإنزيم. يمكن لـ Tn5 الوصول إلى مناطق الكروماتين المفتوحة بشكل أكبرلأنها أقل كثافة من مناطق الكروماتين المغلقة. نتيجة لذلك ، من المرجح أن يقوم Tn5 بإدخال المحولات في مناطق الكروماتين المفتوحة أكثر من مناطق الكروماتين المغلقة. يسمح هذا لـ ATAC-seq باستهداف مناطق الكروماتين المفتوحة في الجينوم وتحديدها بشكل انتقائي. يتم بعدها استخلاص هذه المناطق وسلسلتها. من ميزات هذه التقنية انها تحتاج الى عدد قليل من الخلايا وهي تعتبر الان التقنية الاكثر استعمالا.
- MNase-seq (تسلسل نوكلياز المكورات الدقيقة): تعتمد هذه الطريقة على مبدا معاكس, حيث انها تعتمد على تحديد المناطقة المرتبطة بالهستونات عوض سلسلة المناطق المفتوحة من الجينوم. في هذه الطريقة, يتم استخدام انزيم الـ MNase الذي يقوم بـ"هظم" المناطق المتاحة من الجينوم والتوقف عن مصادفتهم للمناطق الملفوفة حول الهستونات. يمكننا بعدها عزل و سلسلة هذه المناطق و اسنتاج المناطق المتاحة بطريقة غير مباشرة.

رسم بياني يوضح اهم التقنيات المستعملة لدراسة ازاحة الكروماتين (مصدر الصورة بتصرف)
يمكننا تلخيص نوع البيانات المتحصل عليها في الرسم البياني اسفله:
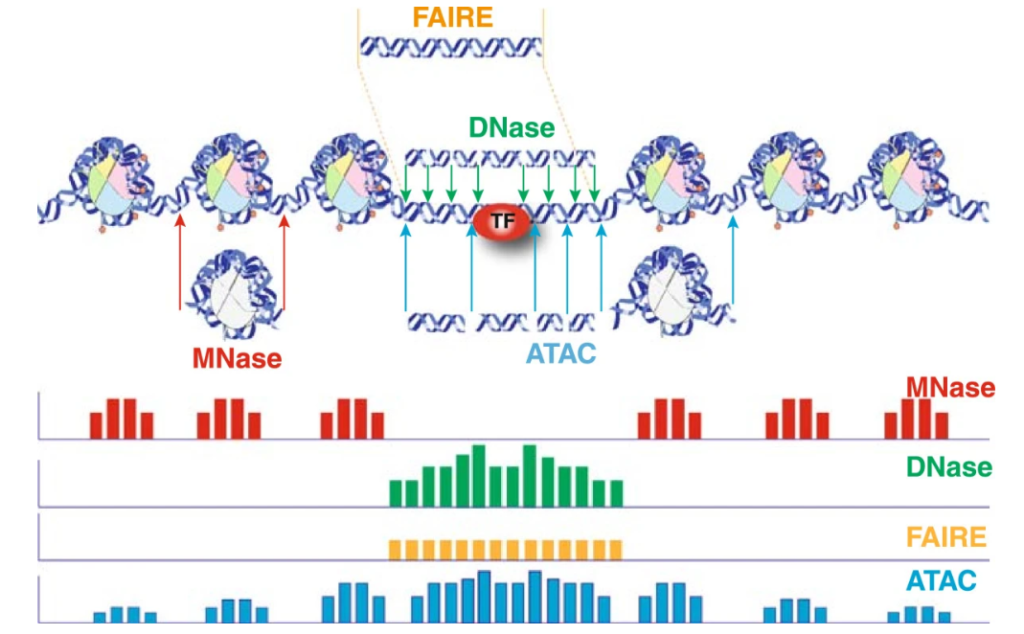
رسم بياني يوضح نوع البيانات التي يتم التحصل عليها من كل تجربة (مصدر الصورة)
الخلاصة
في هذا المقال عرفنا بمجال دراسة ازاحة الكروماتين وعلاقتها بالتعديل الجيني و عرفنا ببعض اهم الطرق المستعملة لدراسة هذا النوع من البيانات. في المقالات القادمة سوف نتكلم باسهاب اكبر عن تقنية ATAC-seq وكيفية تحيليل بياناتها, ثم سوف نتطرق في الى كيفية استعمال هذه الطريقة لدراسة ازاحة الكروماتين على المستوى الخلوي.
وفي الاخير يمكننا تلخيص كل تقنيات الوراثة الآجينية التي تطرقنا لها في هذه المدونة في هذا الرسم البياني:

مصادر
- Thurman, Robert E., et al. "The accessible chromatin landscape of the human genome." Nature 489.7414 (2012): 75-82. <
- Furey, T. S. ChIP-seq and beyond: new and improved methodologies to detect and characterize protein-DNA interactions. Nature reviews. Genetics 13, 840–52 (2012).
- Meyer, C. A. & Liu, X. S. Identifying and mitigating bias in next-generation sequencing methods for chromatin biology. Nature Reviews Genetics 15, (2014).
- Tsompana, M. & Buck, M. J. Chromatin accessibility: a window into the genome. Epigenet Chromatin 7, 33 (2014).
- Risca, V. I. & Greenleaf, W. J. Unraveling the 3D genome: genomics tools for multiscale exploration. Trends in genetics TIG 31, 357–72 (2015).
- Braadland, P. R. & Urbanucci, A. Chromatin reprogramming as an adaptation mechanism in advanced prostate cancer. Endocr-relat Cancer 1, R211–R235 (2019).
- Klemm, S. L., Shipony, Z. & Greenleaf, W. J. Chromatin accessibility and the regulatory epigenome. Nat Rev Genet 20, 207–220 (2019).
- Grandi, F. C., Modi, H., Kampman, L. & Corces, M. R. Chromatin accessibility profiling by ATAC-seq. Nat Protoc 17, 1518–1552 (2022).
رابط المقالة : المعلوماتية الحيوية بالعربية » تقنيات دراسة الاماكن المفتوحة في الجينوم (تنميط اتاحة الكروماتين)